Qualunque informazione fornita su questo sito NON COSTITUISCE un consulto medico e non sostituisce in ogni caso una idonea valutazione del medico. Il contenuto del sito è PURAMENTE a CARATTERE INFORMATIVO. In caso di patologie croniche è bene consultare il proprio medico curante.
Malattie infiammatorie intestinali
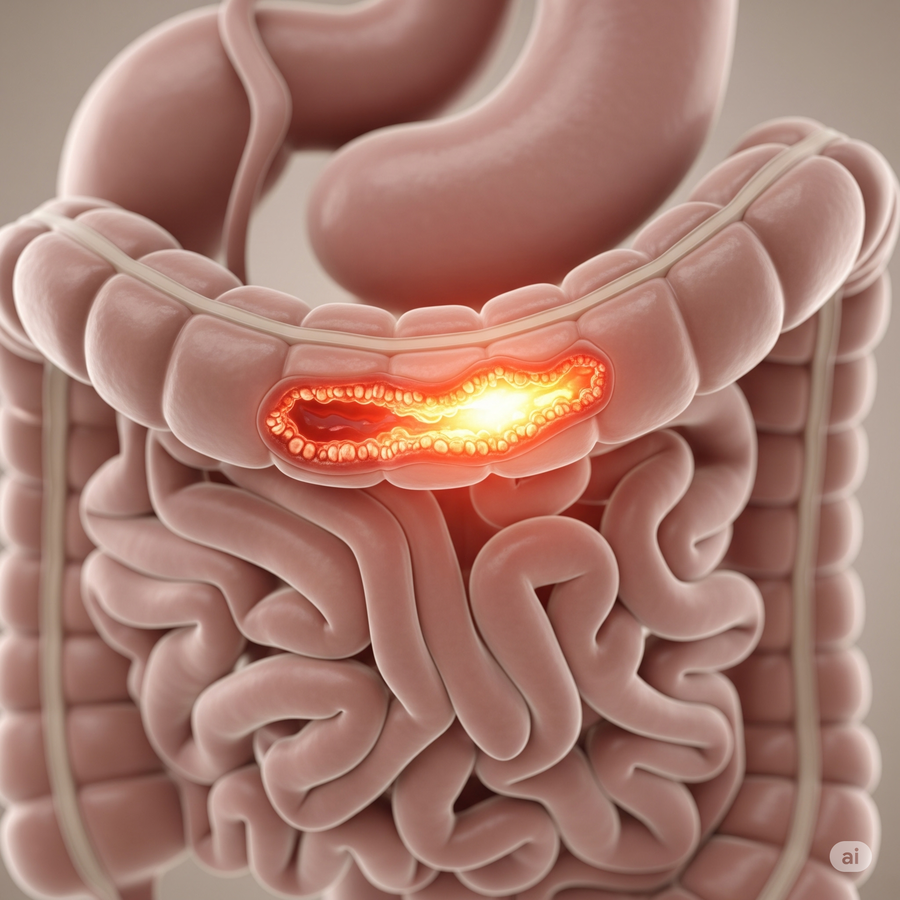
Morbo di Crohn: una patologia autoimmune diffusa ma ancora poco conosciuta